Contenidos
- Virus del Ébola .com
- Síntomas del Ébola
- Cómo se transmite y contagia
- Incubación y efectos
- Prevención del Ébola
- Características del virus del Ébola
- Tratamiento contra el Ébola
- Reservorio y ciclo del virus
- Brotes de Ébola
- Ébola en los Estados Unidos
- Ébola en Europa y España
- Creencias populares y rumores
- Enfermedad Ébola
- Noticias sobre el Ébola
También de interés
Características del virus del Ébola
Tamaño, morfología, estructura, patogenia, cómo se replica, cómo entra en la célula, fisiopatología.
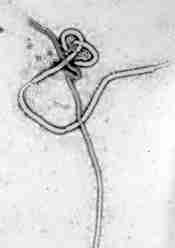 |
La matriz helicoidal está compuesta por las proteínas VP40 y VP24, y comprendida por ranuras transversales de 5 nm. Este conjunto está, a su vez, envuelto por una membrana lipídica en la que van ancladas glicoproteínas GP.
El virus del Ébola tiene un genoma de 19 kilobases con la organización característica de los filovirus. Este genoma codifica nueve proteínas funcionales sobre siete genes. Las variaciones genéticas entre los diferentes virus del género Ebolavirus pueden ilustrarse mediante la comparación del tamaño de los diferentes genomas y sus respectivas tasas de GC (contenido de guanosina-citosina). Por comparación, entre otros filovirus, el virus de Marburg, del género Marburgvirus, tiene un genoma de 19,11 kb de largo con una tasa de GC de 38,8%, mientras que los virus Lloviu, del género Cuevavirus, tienen una longitud genómica de 18.93 kb con una tasa de GC del 46,0%.
Replicación
La fusión de la envoltura del virión con la membrana plasmática de la célula huésped tiene el efecto de liberar la nucleocápside en el citoplasma de la célula diana. La ARN polimerasa L del virus del Ébola se une a un único promotor localizado en el extremo 5' del genoma viral. La expresión génica procede secuencialmente, con el aumento de la probabilidad de interrumpirse a medida que la polimerasa se mueve a lo largo de la cadena de ARN genómico al transcribir. El primer gen a partir del promotor se expresa de este modo.
El orden de los genes en el genoma viral proporciona una manera simple pero eficaz de regular su transcripción: la nucleoproteína NP, codificada por el primer gen, se produce en cantidades mayores que la polimerasa L, codificada por el último gen. La concentración de esta nucleoproteína en el citosol del hospedador determina el momento de la transcripción de la polimerasa L (producción de ARN mensajero a partir del ARN genómico) a la replicación viral (producción de antigenomas de ARN de polaridad positiva por replicación integral de un ARN genómico original completo). Estos antigenomas son, a su vez, transcritos en genomas virales de ARN de polaridad negativa que interactúan con las proteínas estructurales previamente traducidas a partir del ARN viral. Las partículas virales se auto-ensamblan a partir de proteínas y de material genético recién producido cerca de la membrana celular. Brotan de la célula en forma de envoltura viral hecha de membrana plasmática, donde se insertan las glicoproteínas GP, liberando nuevos viriones listos para infectar a otras células.
Expresión de la glicoproteína
La glicoproteína GP juega un papel determinante en la virulencia del virus del Ébola. Se expresa normalmente en forma soluble sGP de 364 residuos de aminoácidos que forman un homodímero de 110 kDa compuesto por dos cadenas polipeptídicas idénticas paralelas, ensambladas por dos puentes disulfuro al nivel de las cisteínas 53 y 30629. El producto de la transcripción del gen GP es, en realidad, ligeramente más largo que la proteína sGP funcional, que resulta de la escisión por una furina de la pre-sGP producida, liberando una pequeña proteína no estructural y fuertemente O-glicosilada llamada Δ-péptido (o péptido Δ).
Sin embargo, el gen GP del género Ebolavirus contiene siete residuos de adenina consecutivos que forman una estructura de horquilla, o tallo-bucle, al nivel de la cual la polimerasa viral patina o "tartamudea" (se conoce como tartamudeo de la polimerasa). Aproximadamente en uno de cada cinco casos se inserta una adenina extra en el ARN mensajero, que desplaza un nucleótido el marco de lectura de los codones por el ribosoma. La proteína producida por este ARNm modificado, la GP propiamente dicha, es, pues, diferente de la sGP: sus 295 residuos N-terminales son idénticos, pero los siguientes 312 residuos secundarios, C-terminales, son diferentes. De ello se desprende una proteína más larga, con un total de 676 residuos (uno más para el virus Reston), escindida por una furina a nivel de una región básica para formar dos subunidades, GP1 y GP2, unidas por un puente disulfuro entre la Cys53 de la GP1 y la Cys609 de la GP2. Este heterodímero se ensambla en trímero de 450 kDa a la superficie de la membrana lipídica de los viriones y permite la penetración en las células huésped para infectar.
El patinaje de la polimerasa L en la horquilla también produce una glicoproteína terciaria, llamada ssGP, cuya función no se conoce y que se cree que es monomérica. Esto ocurre mediante la inserción de dos residuos de adenina extra a nivel de la región tallo-bucle del gen GP del virus, que desplaza dos nucleótidos el marco de lectura del ARNm para el ribosoma y genera una proteína de 298 residuos de aminoácidos.
La expresión de varias glicoproteínas por superposición de genes es una característica para distinguir, entre los filoviruses, los virus de los géneros Ebolavirus y Cuevavirus del virus Marburgvirus, con esta última especie produciendo sólo glicoproteína GP.
Acción patógena
Al igual que otros filovirus, el virus del Ébola ataca todo el cuerpo provocando una creciente coagulación intravascular diseminada, que degrada rápidamente la hemostasia y el funcionamiento de los órganos vitales. La infección se dirige principalmente a las células endoteliales, los fagocitos mononucleares (monocitos, macrófagos, células dendríticas, mastocitos) y los hepatocitos. Se acompaña de la neutralización rápida de ciertas poblaciones de linfocitos T por un superantígeno.
Una vez que el virus está en la célula, segrega la glicoproteína soluble sGP y la glicoproteína estructural GP. La replicación del virus satura la síntesis de proteínas en las células infectadas, particularmente las del sistema inmune del huésped. La glicoproteína GP forma un complejo trimérico que une el virus a las células endoteliales que tapizan el interior de los vasos sanguíneos, mientras que la glicoproteína secretada sGP forma un dímero que interfiere con los granulocitos neutrófilos, un tipo de glóbulos blancos, permitiendo que el virus escape al sistema inmune del huésped por inactivación precoz de los neutrófilos. Estos leucocitos inactivados sirven entonces como portadores del virus del Ébola por todo el cuerpo, contaminando los ganglios linfáticos, el hígado, el pulmón y el bazo. La presencia de partículas virales, y los daños causados a las células por la eclosión, provocan la liberación de citoquinas (TNFα, IL-6, IL-8, etc), que son las moléculas de señalización celular que causan fiebre e inflamación. El daño a las células epiteliales por efecto citopático conduce a la pérdida de la integridad vascular, agravado por un lado por la glicoproteína viral que reduce la eficacia de las integrinas responsables de la adherencia de las células en las estructuras intercelulares, y en segundo lugar por el daño hepático responsable de la coagulopatía.